干细胞“补丁”修复心脏!科学家首次在灵长类和人类中实现心肌再生
心力衰竭是全球主要致死疾病之一,传统治疗手段有限。近日,一项发表在《Nature》杂志上的突破性研究通过诱导多能干细胞(iPSC)技术,成功在恒河猴心衰模型和人心衰患者中实现心肌再生,为心脏修复开辟了全新路径。
心脏修复的“终极挑战”
心肌细胞是人体内高度分化的细胞,不具备再生能力,因此一旦发生急性或慢性缺血,心肌会受到不可逆转的损伤,最终导致心力衰竭。传统治疗依赖药物或心脏移植,但供体稀缺且免疫排斥风险高。干细胞疗法被视为最具潜力的解决方案,目前已有研究将体外培养获得的心肌细胞植入心脏,使衰竭的心脏恢复活力。但如何让移植的心肌细胞长期存活并持续发挥治疗功能,并避免心律失常及肿瘤形成仍是科学界和医学界的重大挑战。
神奇的“心脏补丁”:EHM移植物
Wolfram-Hubertus Zimmermannj及其研究团队,将通过诱导多能干细胞(iPSC)技术,将成体细胞重编程为心肌细胞(CMs)和基质细胞(StCs)。将分化后的 CMs 和 StCs 按比例与胶原水凝胶混合后,形成初始混合物。该细胞-水凝胶混合物被加入到3D打印特定形状的模具中,通过含生长因子的培养基进行28天以上的培养,得到可收缩的工程化心肌(EHM)贴片。
这种工程化心肌能够以“贴片补丁”的形式,移植到左心室前壁至心尖的心外膜区域,对受损心肌进行修复。其具有三大优势:
² 结构仿生:模拟天然心肌的三维结构,心肌细胞为主,基质细胞提供结构支持,与水凝胶材料的结合增强了工程化心肌的机械稳定性;
² 功能整合:工程化心肌通过机械耦合而非电传导改善心脏收缩力,有效减少宿主心律失常的风险;
² 免疫兼容:结合免疫抑制方案,有效降低排斥反应;
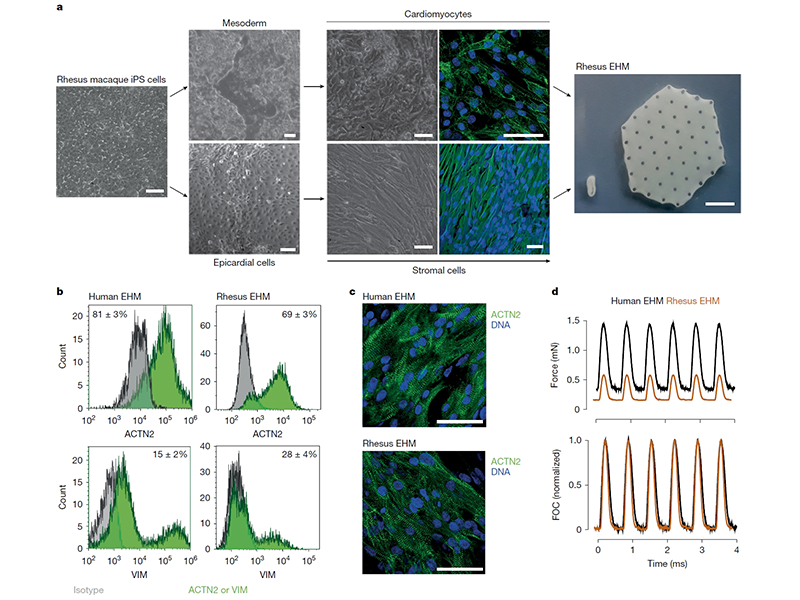
工程化心肌(EHM)的制备过程,EHM的具有完整的肌节结构,并能够产生规律的收缩力

工程化心肌EHM可产生规律收缩
从恒河猴到人类:跨物种验证的里程碑
研究者首先在健康的恒河猴模型上进行安全性评价,结果显示长达168天的安全性研究中,并未发现肿瘤和严重的心律失常情况。同时,他克莫司和甲泼尼龙联用的免疫抑制方案,能够有效控制移植物所带来的免疫排斥反应。
随后,研究者通过缺血再灌注的方法,建立了心衰的恒河猴模型,将EHM贴覆于心外膜受损部位,并通过TachoSil膜辅助的方式,提高对EHM的机械支持。低剂量组移植2张EHM(8千万细胞),高剂量组移植5张EHM(2亿细胞)。
结果显示,接受EHM移植的低剂量组恒河猴心脏壁增厚1.4毫米;高剂量组恒河猴的心脏壁增厚21%,左心室射血分数(LVEF)提升7%,纤维化面积显著降低,心功能得到了明显改善。
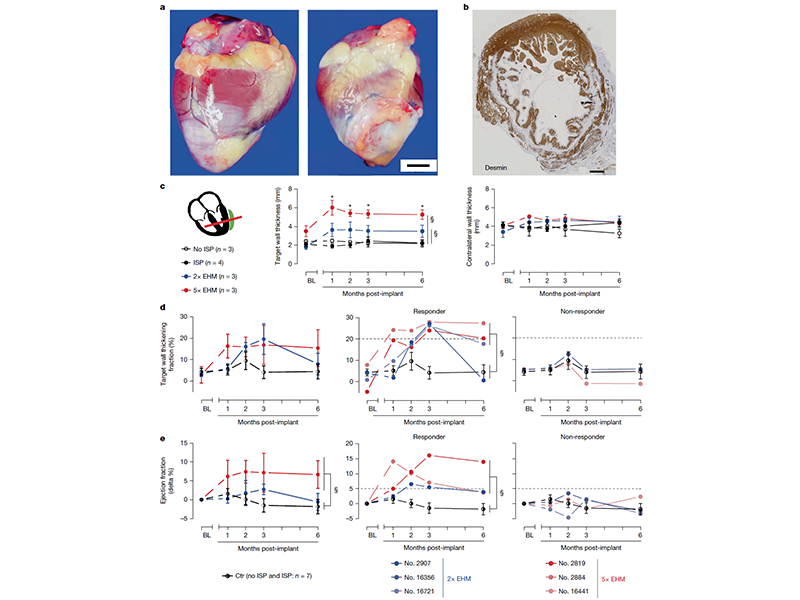
工程化心肌(EHM)异体移植物通过再血管化增强局部和整体心脏功能,在慢性心力衰竭恒河猴模型中呈现剂量依赖性疗效。

人源iPSC制备的EHM收到机械刺激后产生收缩
人类首例:临床转化的关键一步
一名46岁的女性晚期心力衰竭患者(NYHA分级为III级)接受了由同种异体脐带血细胞重编程分化制备得到的EHM。10张EHM移植至左心室前壁至心尖的心外膜区域,覆盖梗死瘢痕。在3个月的随访期内,LVEF从35%提升至39%,左室舒张末期容积(LVEDV)从104mL下降至78mL,左室收缩末期容积(LVESV)从68mL下降至48mL。整体评价心脏功能得到了恢复。
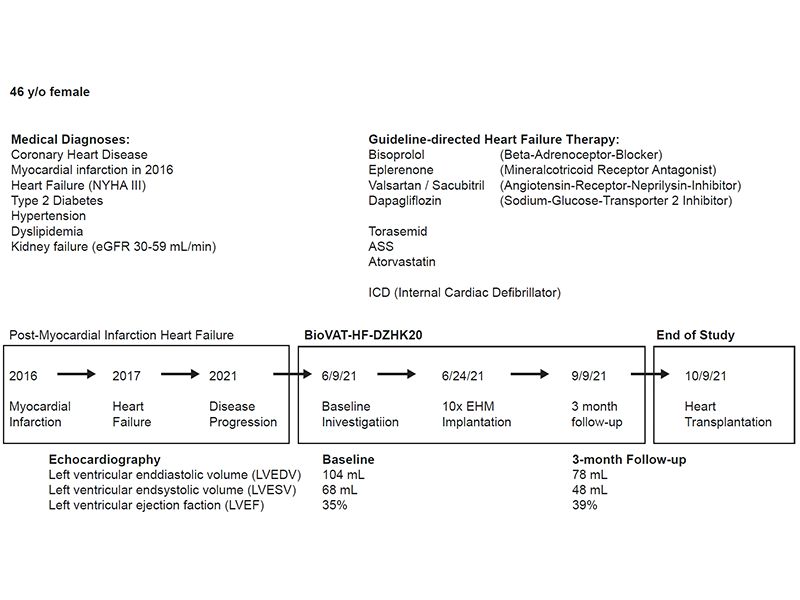
首例临床患者基本情况、治疗方案及随访结果
未来展望:挑战与希望并存
这项研究不仅是再生医学的里程碑,更是心力衰竭患者的曙光。从已有的恒河猴研究结果显示,EHM的移植成功整合到宿主心肌中,虽然心肌细胞未完全成熟,但形成了功能性连接。这为患者争取了等待心脏移植的宝贵时间。
参考资料
Jebran, A.-F., et al. (2025). Engineered heart muscle allografts for heart repair in primates and humans. *Nature*.
-
干细胞“补丁”修复心脏!科学家首次在灵长类和人类中实现心肌再生
心力衰竭是全球主要致死疾病之一,传统治疗手段有限。近日,一项发表在《Nature》杂志上的突破性研究通过诱导多能干细胞(iPSC)技术,成功在恒河猴心衰模型和人心衰患者中实现心肌再生,为心脏修复开辟了全新路径。2025年03月12日 -
干细胞技术助力解锁特发性肺纤维化(IPF)细胞模型构建
特发性肺纤维化(IPF,idiopathic pulmonary fibrosis)是一种致死率很高的疾病,每10万人中就有3-45人受其困扰,患者的中位生存期仅有3-4年。2025年02月28日 -
血管基质成分(SVF):骨关节炎治疗新曙光
是否曾在上下楼梯时,膝盖传来一阵酸痛?或是在久坐起身时,关节仿佛被“卡住”动弹不得?2025年02月20日
