MSC药物的奥秘探寻:药代动力学与药效机制解析
间充质干细胞(Mesenchymalstemcell,MSC)疗法作为处在医学研究与临床治疗的前沿领域一直备受瞩目,近期美国食品药品监督管理局(FDA)和中国国家药品监督管理局(NMPA)先后各批准了一款MSC药物上市,再次让更多人的目光聚集到MSC上。MSC药物作为一种细胞药,比小分子药物和大分子药物在生产制备、存储运输方面具有更高的难度。另一方面,MSC药物的药代动力学、起效机理与既有药物有较大不同。这里将参考已经发表的科学文章,以最常见的静脉给药方式为代表,对MSC通过静脉进入人体后的药代动力学和药效进行探讨。
MSC进入人体后的分布与时效
一项针对肝硬化患者的临床研究使用示踪素111In-oxine标记MSC后通过静脉给药的方式进入患者体内,每名患者的给药量在2.3-4亿。而后通过PET-CT进行长达10天的观察追踪,研究MSC在体内分布的动态变化。结果显示,在细胞输注初期,肺部成为MSC的首要聚集部位。这是由于肺部微血管网络复杂且毛细血管直径较小,大量MSC在首次通过肺部循环时被截留。随着时间推移,肺内MSC残余活性逐渐降低,从输注后2小时的27.0-33.5%降低至第10天的2.0-5.4%。
肝脏和脾脏的MSC积累在输注后2-4小时逐渐显现。除部分特殊病例外,多数患者肝脏和脾脏放射性摄取在2小时后才被检测到。并且MSC在肝脏和脾脏的放射性信号持续增强。从量化数据来看,肝脏细胞百分比在输注后从近乎0增长至第10天的13.0-17.4%,而脾脏残余活性从较低水平攀升至30.1-42.2%,这显示出脾脏对MSC的捕获与滞留能力。这一差异可能与肝硬化患者脾肿大及门静脉高压引发的血流动力学改变密切相关,此类病理变化改变了局部微环境相关。
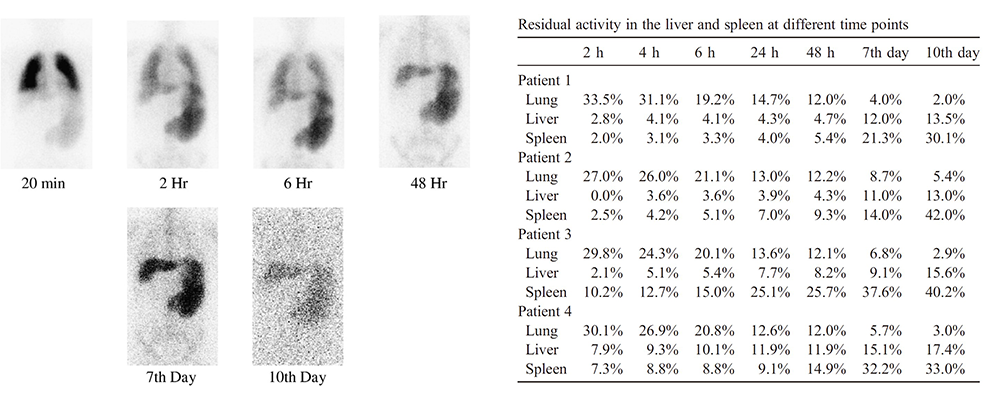
MSC经静脉进入人体后的动态分布及在肺、肝、脾的存留活性[1]
MSC的药代动力学模型
一项使用小鼠作为模型动物的研究中,将MSC用绿色荧光蛋白进行标记后经静脉输注至小鼠体内,从而构建的药代动力学动物模型,以揭示MSC在体内运输、分布与消除的复杂过程。
其结果显示,MSC注入静脉后,受不同器官血流速度及血管结构影响,其在体内的迁移路径与数量分布各异。抵达器官时,因自身较大体积及与血管内皮细胞的相互作用,MSC部分被微血管截留,部分黏附于内皮壁。肺部微血管结构特殊,致使其截留率常数较高,成为限制MSC早期全身分布的关键因素;而在肝脏等器官,截留的MSC可能在特定代谢与信号传导条件下重新释放入血,继续循环,且各器官释放速率受自身代谢环境等因素调控,存在显著差异。
在消除过程中,MSC在血液及器官内遵循一级动力学规律逐渐消耗清除。血液中较高的消耗率常数凸显其在MSC消除进程中的关键作用,肾脏凭借强大的过滤与代谢功能,在各器官中消耗率常数居前,细胞凋亡、代谢紊乱及免疫系统识别清除等多种机制协同参与,共同塑造了MSC在体内的存活曲线与数量动态变化,这些机制在不同器官中的作用程度差异成为影响MSC体内命运的核心要素。
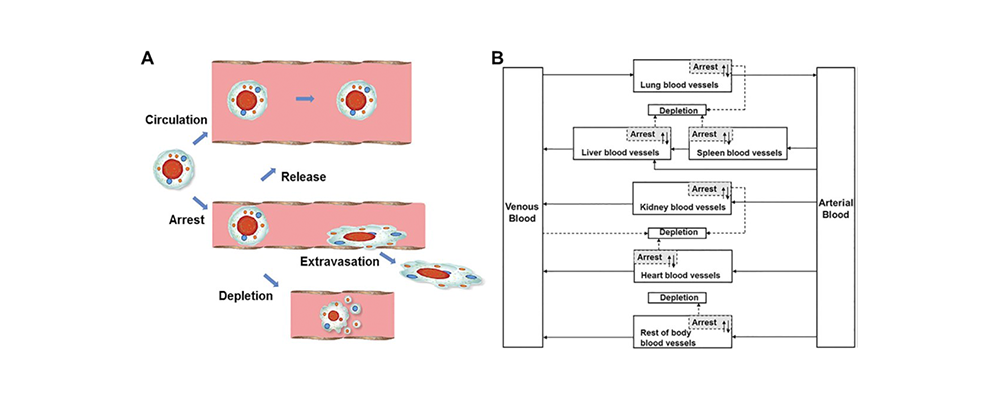
MSC在体内的药代动力学假说和模型[2]
MSC的归巢机理
MSC归巢至靶器官是一个多步骤精细调控过程。初始阶段,MSC表面配体与血管内皮细胞表达的选择素结合,引发细胞在血管壁的滚动,此过程中整合素发挥关键作用。如血管细胞粘附分子-1(VCAM-1)与CD29结合,在适宜剪切应力下促进MSC快速滚动,而CD49d表达不足会削弱这一过程,影响归巢效率。随后,趋化因子超家族成员与MSC上的G蛋白偶联趋化因子受体相互作用,激活MSC,增强整合素依赖性粘附,促使细胞稳定结合于内皮细胞,并引导其迁移方向。同时,MSC分泌基质金属蛋白酶降解基底膜与细胞外基质,助力细胞穿越内皮屏障,完成归巢,各环节紧密相连,任何一步异常都可能干扰归巢效果。
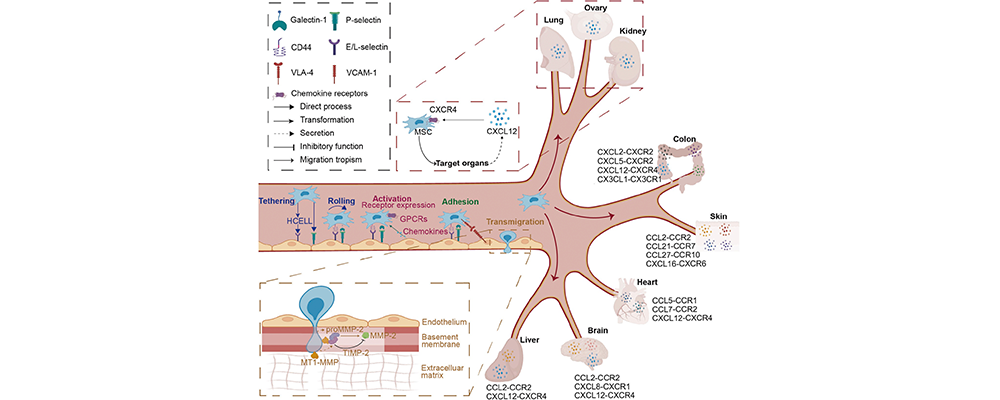
MSC通过静脉进入血管后,经过锚定/滚动、激活、贴附、迁移过程,受趋化因子介导至目的器官/组织[3]
MSC的代谢结局与清除途径
MSC回输后在体内并非持久存在,其清除过程迅速,报道显示存活时间从28小时到120天不等,且起始肺部聚集现象在一天内便会消散,其代谢终点呈现多元化特征。凋亡是常见途径之一,可由细胞内源性程序启动,独立于外部病理环境的毒性与排异反应。自噬MSC在静脉给药后由细胞饥饿、炎症、氧化应激(ROS)共同导致的。对于分化这一细胞终局,虽然有相关文献报道,但当前主流观点对此存疑,如2024年《Nature》杂志撤回相关文章,使得分化在MSC命运中的地位备受争议。此外,铁死亡因细胞内铁过载与脂质过氧化加剧而发生。吞噬作用也是MSC的清除途径之一。肺部单核细胞率先吞噬MSC,随后部分MSC转移至肝脏等组织,受到各组织内巨噬细胞在不同时段的吞噬。细胞分裂及ROS积累引发的衰老现象同样是MSC代谢的可能结局,这些不同代谢途径相互交织,共同决定了MSC在体内的存续与功能发挥。
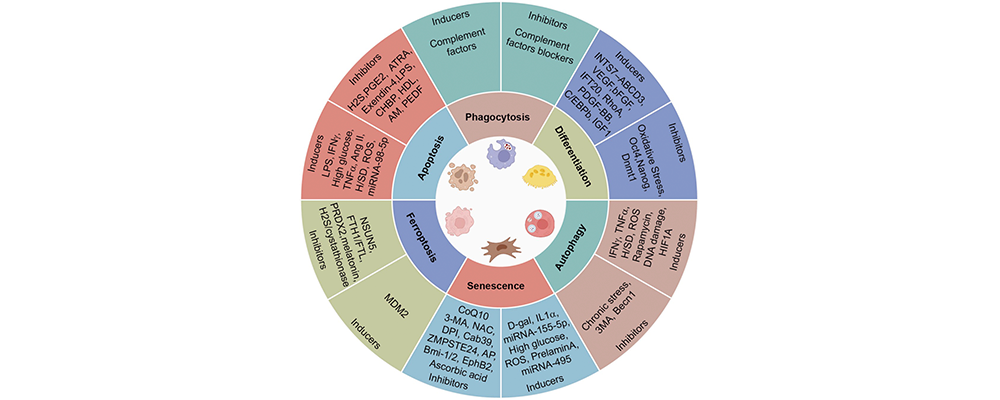
MSC的代谢结局及相关调控因素[3]
MSC的药效机理假说
诸多已发表文献均对MSC的免疫调节作用和促血管形成能力进行了体内外的分析评价。但很难向小分子药物一样针对某一靶点做出针对性机理。目前对于MSC药物药效理论假说是“shotgunmodel”(霰弹理论),即MSC通过多个靶点和机制对机体发挥调节作用,以维持机体的平衡稳态,而不是通过单一靶点和简单的促进或抑制作用。对于MSC的迁移、归巢及代谢,“hit-and-run”(or“touchandgo”)机理认为,MSC快速迁移至受损组织、短暂释放治疗分子后迅速清除但长效维持治疗效果的特性。
在MSC药物的研究与应用进程中,诸多难题亟待攻克,如来细胞供体样本的异质性所带来的起始原材料差异、超长的生产制备流程所带来的控制风险,以及较大的临床示踪难度所带来的药代动力学检测难题。目前已经进入临床试验阶段的MSC产品或技术已经很多,如何突破这些瓶颈,优化MSC药物研发与应用策略,是未来干细胞医药研究的核心任务之一。这里不仅需要须整合多学科力量,建立创新的研究方法与技术,同时也需要上下游产业端的贯通和融合,加速MSC药物从实验室到临床治疗、从针对少数个体的医疗技术到货架型细胞药物的进程。
参考文献:
[1] Gholamrezanezhad A, Mirpour S, Bagheri M, et al. In vivo tracking of 111In-oxine labeled mesenchymal stem cells following infusion in patients with advanced cirrhosis. Nucl Med Biol. 2011;38(7):961-967.
[2] Wang H, Liang X, Xu ZP, Crawford DH, Liu X, Roberts MS. A physiologically based kinetic model for elucidating the in vivo distribution of administered mesenchymal stem cells. Sci Rep. 2016;6:22293.
[3] Shan Y, Zhang M, Tao E, et al. Pharmacokinetic characteristics of mesenchymal stem cells in translational challenges. Signal Transduct Target Ther. 2024;9(1):242. Published 2024 Sep 13.
-
干细胞“补丁”修复心脏!科学家首次在灵长类和人类中实现心肌再生
心力衰竭是全球主要致死疾病之一,传统治疗手段有限。近日,一项发表在《Nature》杂志上的突破性研究通过诱导多能干细胞(iPSC)技术,成功在恒河猴心衰模型和人心衰患者中实现心肌再生,为心脏修复开辟了全新路径。2025年03月12日 -
干细胞技术助力解锁特发性肺纤维化(IPF)细胞模型构建
特发性肺纤维化(IPF,idiopathic pulmonary fibrosis)是一种致死率很高的疾病,每10万人中就有3-45人受其困扰,患者的中位生存期仅有3-4年。2025年02月28日 -
血管基质成分(SVF):骨关节炎治疗新曙光
是否曾在上下楼梯时,膝盖传来一阵酸痛?或是在久坐起身时,关节仿佛被“卡住”动弹不得?2025年02月20日
