干细胞疗法能否成为改善糖尿病的新希望?
糖尿病已成为全球公共卫生问题,对人类健康和社会经济造成了巨大的负担。2021年,中国糖尿病发病人数超过400万,糖尿病患病总人数超过1.17亿,死亡人数超过17万例[1]。同时,糖尿病患者在长期控糖不佳的情况下,还有一系列并发症,如急性的糖尿病酮症酸中毒和高渗高血糖综合征,以及慢性的心血管疾病、视网膜病变、肾病变、下肢血管病变、周围神经病变、糖尿病足溃疡等,均会不同程度地影响糖尿病患者的生活质量甚至危及生命。
糖尿病的分类及流行病学特点
根据糖尿病的发病机制,通常将其可以分为1型糖尿病,2型糖尿病,妊娠糖尿病和特殊类型糖尿病四类。
1型糖尿病是一种自身免疫病,免疫系统错误地攻击并破坏胰腺中的胰岛β细胞,导致胰岛素分泌绝对不足。1型糖尿病多发生在儿童和青少年,也可发生于各种年龄段。流行病学特点方面,1型糖尿病在全球范围内均有发病,但发病率存在明显的地区差异。在北欧等地区发病率较高,而在亚洲、非洲等地区相对较低,在中国1型糖尿病患者比例占糖尿病总患病人群的不到1%。
2型糖尿病是最常见的糖尿病类型,约占糖尿病患者总数的90%以上。发病与遗传因素和环境因素密切相关,主要由于胰岛素抵抗和胰岛β细胞功能减退所致。胰岛素抵抗指身体细胞对胰岛素的敏感性降低,使得胰岛素促进葡萄糖摄取和利用的效率下降,进而血糖升高。随着病情进展,胰岛β细胞功能逐渐衰退,胰岛素分泌也逐渐减少。肥胖、体力活动不足、不健康饮食、衰老都是2型糖尿病的重要危险因素。流行病学特点方面,2型糖尿病的发病率在全球范围内呈快速上升趋势,尤其在发展中国家更为显著。这与经济发展带来的生活方式改变,如高热量饮食摄入增加、运动量减少等密切相关。在我国,2型糖尿病患者数量庞大,且发病年龄逐渐年轻化。
妊娠糖尿病因妊娠期间激素水平变化抵抗胰岛素作用,致胰岛素敏感性下降,多数患者分娩后血糖可恢复正常。特殊类型糖尿病的病因复杂多样,包括基因缺陷、外部创伤、内分泌疾病、药物使用、感染以及其他遗传因素等。特殊类型糖尿病相对较少见,发病率较低。
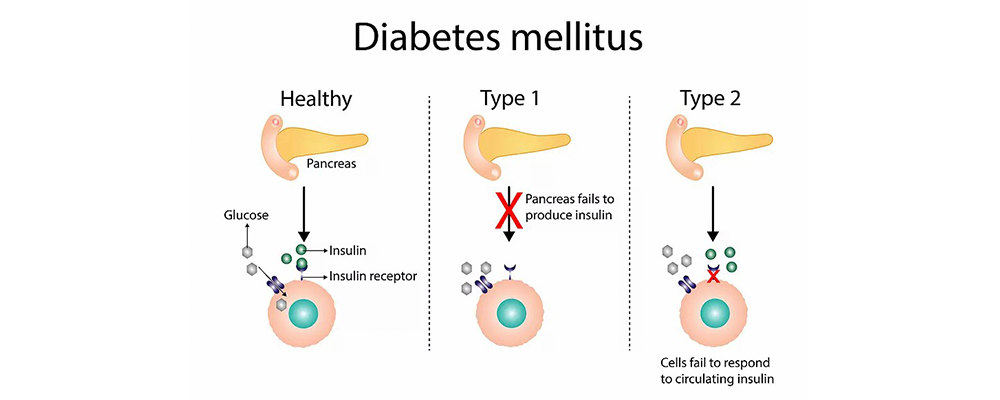
1型糖尿病与2型糖尿病患者胰岛素分泌和起效原理图(图片来源于www.hotzehwc.com)
MSC治疗糖尿病的机理研究
间充质干细胞(MesenchymalStemCell,MSC)具有良好的免疫调节、改善胰岛素抵抗、促进胰岛素产生和辅助胰岛功能。从根本上能够对1型糖尿病和2型糖尿病起到治疗效果。根据已有的动物试验研究结果,MSC能够从以下几个方面对糖尿病进行干预:
MSC对1型糖尿病治疗的机理
免疫调节保护胰岛:MSC能够抑制自身反应性T细胞增殖和活化,降低胰岛炎症水平。在NOD小鼠模型中可以观察到胰腺中TNF-α表达降低,TGF-β1和IL-10表达升高,同时增加脾调节性T细胞(Tregs)比例,减少CD8⁺T细胞比例和血浆促炎介质水平。还能促进Tregs形成,维持免疫耐受,防止对胰岛β细胞的自身免疫攻击。
促进胰岛β细胞功能:增强胰腺微环境,减少β细胞凋亡并支持其存活,如脐带来源MSC与利拉鲁肽联合使用可抑制T2D模型中β细胞凋亡;分泌营养介质和生长因子促进血管生成,改善β细胞营养供应,如分泌VEGF、FGF等促进胰岛血管生成。
改善代谢指标,减少并发症影响:MSC注射后能够提高血清胰岛素和C肽水平,改善葡萄糖耐量,这在多种动物模型中均得到证实。另外,MSC分泌的营养相关因子可修复肾损伤,改善糖尿病相关并发症。
MSC对2型糖尿病治疗的机理
改善胰岛素抵抗:促进脂肪组织巨噬细胞或胰岛内巨噬细胞从 M1 促炎表型向 M2 抗炎表型极化,同时调节胰岛素信号通路相关分子(如增强 IRS - 1 磷酸化、促进 GLUT4 表达和转位等),增强外周组织对胰岛素的敏感性,降低胰岛素抵抗,多种模型已观察到相关分子和代谢指标变化。
调节代谢功能:调节肝脏葡萄糖和脂质代谢,如抑制肝糖原分解、减少糖异生、改善血脂异常等;促进胰岛β细胞功能恢复,包括增加胰岛素分泌、改善GK大鼠胰岛形态和功能、逆转db/db小鼠β细胞去分化等。
减轻炎症反应:降低系统性炎症水平,减少炎症细胞浸润和炎症因子分泌,如ASCs可降低糖尿病小鼠血清中IL-6、TNF-α等炎症因子水平,增加抗炎因子IL-10水平;抑制NLRP3炎性小体激活,减轻炎症损伤。
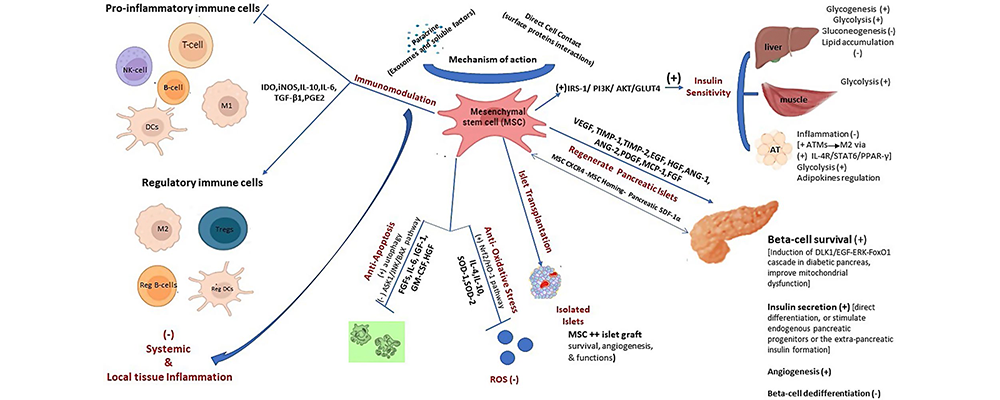
MSC在糖尿病治疗中的治疗机制(图片来源于参考资料[2])
MSC在临床的应用效果
目前有一定数量的临床研究使用MSC治疗1型糖尿病和2型糖尿病。埃及开罗大学的研究者发表了对现有临床试验的相关综述[2],部分研究结果总结如下:
自体MSC对于1型糖尿病患者有一定的治疗效果,通过静脉注射自体骨髓来源MSC后,1年的混合餐耐量试验中的C肽反应得到显著改善,表明其对疾病进程有干预作用且能保护β细胞功能[3];在另一组患者中,从第一个月起每日胰岛素剂量有所降低,但糖化血红蛋白(HbA1c)和瘦素水平变化相对较小,到第三个月瘦素水平显著升高[4]。异体MSC对1型糖尿病患者也有一定的治疗潜力。使用异体脐带来源MSC对15例新发病的1型糖尿病患者进行治疗,并进行24个月随访,受试者餐后血浆葡萄糖和HbA1c显著降低,同时空腹C肽(FCP)显著增加,约20%患者停用外源性胰岛素,超半数患者胰岛素剂量大幅降低[5]。另一项使用异体骨髓来源MSC治疗5例伴有酮症酸中毒的1型糖尿病患者的研究显示,4例患者对治疗有响应,表现为至少三年HbA1c水平降低,FCP或餐后血浆C肽(PCP)下降速度减慢,3例患者至少两年平均每日胰岛素剂量降低超40%[6]。
自体MSC用于2型糖尿病的临床研究较少,异体MSC表现出良好的效果。1项使用牙髓来源MSC治疗的临床数据显示,MSC治疗可有效改善代谢指标及胰岛功能,且研究发现患者治疗前的血糖、血脂水平和胰岛功能越好(HbA1c<8.5、总胆固醇<5mmol/L、甘油三酯≤1.5mmol/L或低密度脂蛋白胆固醇<3.2mmol/L),其对MSC的治疗敏感性越高,表现为胰岛素使用剂量显著降低[7]。从而说明了早期2型糖尿病患者能够从MSC治疗中获得更大收益。胎盘来源MSC静脉注射在治疗6个月后,可显著降低患者平均每日胰岛素剂量和HbA1c水平,同时C肽显著增加,肾功能和心功能也得到改善[8]。脐带来源MSC静脉注射治疗T2D患者,3年后PPG和HbA1c水平显著降低,FCP显著增加,部分患者胰岛素剂量减少或停用,且与对照组相比并发症发生率显著降低[9]。解放军总医院利用脐带来源MSC治疗2型糖尿病患者的随机双盲试验结果显示,MSC能够有效降低糖尿病患者的胰岛素抵抗,治疗48周后,干细胞治疗组20%的病人达到了HbA1c低于7.0%,每天胰岛素用量减半。安慰剂组仅有4.55%的患者能够达到该效果。13.57%的患者在使用干细胞1-3个月,能够达到不使用胰岛素的效果,且能够维持最多至1年的时间。有5名患者完全摆脱胰岛素使用[10]。
其他干细胞治疗糖尿病的临床研究
诱导多能干细胞技术(induced pluripotent stem cell,iPSC)则通过直接分化成胰岛细胞,对1型糖尿病及胰岛素依赖的2型糖尿病实现胰岛功能替代。目前该研究也进入临床研究阶段。2024年天津市第一中心医院联合北京大学,以脂肪来源MSC作为起始细胞,用化学诱导方式得到iPSC,并分化成胰岛细胞。随后胰岛细胞被移植至患者腹直肌前鞘下。患者术后75天脱离胰岛素,血糖控制良好且无严重低血糖事件,目前疗效已稳定持续1年以上[11]。此外,海军军医大学第二附属医院联合中国科学院分子细胞科学卓越创新中心利用2型糖尿病患者的外周血单个核细胞建立iPSC细胞系,在体外诱导建立与成体胰岛相近的再生胰岛组织E-islets后将该组织植入到患者肝脏内。术后11周患者完全脱离外源胰岛素,口服降糖药也逐步减量,并在术后一年左右实现撤药,目前该患者已彻底脱离胰岛素33个月[12]。
综上所述,MSC通过调节体内稳态环境,降低炎症反应,提高机体代谢功能的方式,让糖尿病患者的病情得到缓解。MSC在糖尿病治疗的临床前研究与临床应用中已取得一定成果,积累了较多的临床数据,但仍面临诸多挑战。现有临床试验大多处于I期及II期,未来还需开展更多大规模、多中心、高质量的临床实验,验证MSC并深入剖析其作用机制,优化治疗方案。iPSCs技术通过直接分化成胰岛细胞的方式,实现胰岛功能替代也进入临床研究阶段,未来仍需进行更深入的研究及更多临床数据的积累,排除成瘤性及潜在排异反应情况。相信随着技术和产业的协同发展,干细胞技术将能够在糖尿病治疗领域有稳步发展,安全有效地改善糖尿病患者生活质量,从而减轻社会医疗负担,为广大糖尿病患者带来新的希望曙光。
参考资料:
[1] Deng W, Zhao L, Chen C, et al. National burden and risk factors of diabetes mellitus in China from 1990 to 2021: Results from the Global Burden of Disease study 2021. Journal of Diabetes. 2024;16(10):e70012.
[2] Alaa Zeinhom, Sahar A. Fadallah, Marwa Mahmoud. Human mesenchymal stem/stromal cell based-therapy in diabetes mellitus: experimental and clinical perspectives. Stem Cell Research & Therapy (2024) 15:384.
[3] Carlsson PO, Schwarcz E, Korsgren O, Le Blanc K. Preserved beta-cell functionin type 1 diabetes by mesenchymal stromal cells. Diabetes. 2015;64:587–92.
[4] Ulyanova O, Askarov M, Kozina L et al. Autologous mesenchymal stem cell transplant in patients with type 1 diabetes Mellitus. Exp Clin Transpl. 2019;17:236–8.
[5] Hu J, Yu X, Wang Z et al. Long term effects of the implantation of Wharton’s jelly-derived mesenchymal stem cells from the umbilical cord for newly-onset type 1 diabetes mellitus. Endocr J. 2013;60:347–57.
[6] Li L, Hui H, Jia X et al. Infusion with human bone marrow-derived mesenchymal stem cells improves beta-cell function in patients and non-obese mice with severe diabetes. Sci Rep. 2016;6:37894.
[7] Li W, Jiao X, Song J et al. Therapeutic potential of stem cells from human exfoliated deciduous teeth infusion into patients with type 2 diabetes depends on basal lipid levels and islet function. Stem Cells Transl Med. 2021;10:956–67.
[8] Jiang R, Han Z, Zhuo G et al. Transplantation of placenta-derived mesenchymal stem cells in type 2 diabetes: a pilot study. Front Med. 2011;5:94–100.
[9] Hu J, Yu X, Wang Z et al. Long term effects of the implantation of Wharton’s jelly-derived mesenchymal stem cells from the umbilical cord for newly-onset type 1 diabetes mellitus. Endocr J. 2013;60:347–57.
[10] Li Zang, Yijun Li, Haojie Hao et al. Efficacy and safety of umbilical cord‑derived mesenchymal stem cells in Chinese adults with type 2 diabetes: a single‑center, double‑blinded, randomized, placebo‑controlled phase II trial
[11] Wang S, Du Y, Zhang B, et al. Transplantation of chemically induced pluripotent stem-cell-derived islets under abdominal anterior rectus sheath in a type 1 diabetes patient. Cell. 2024;187(22):6152-6164
[12] Wu J, Li T, Guo M, et al. Treating a type 2 diabetic patient with impaired pancreatic islet function by personalized endoderm stem cell-derived islet tissue. Cell Discov. 2024;10(1):45.
-
干细胞“补丁”修复心脏!科学家首次在灵长类和人类中实现心肌再生
心力衰竭是全球主要致死疾病之一,传统治疗手段有限。近日,一项发表在《Nature》杂志上的突破性研究通过诱导多能干细胞(iPSC)技术,成功在恒河猴心衰模型和人心衰患者中实现心肌再生,为心脏修复开辟了全新路径。2025年03月12日 -
干细胞技术助力解锁特发性肺纤维化(IPF)细胞模型构建
特发性肺纤维化(IPF,idiopathic pulmonary fibrosis)是一种致死率很高的疾病,每10万人中就有3-45人受其困扰,患者的中位生存期仅有3-4年。2025年02月28日 -
血管基质成分(SVF):骨关节炎治疗新曙光
是否曾在上下楼梯时,膝盖传来一阵酸痛?或是在久坐起身时,关节仿佛被“卡住”动弹不得?2025年02月20日
